Mini-Herz aus dem Labor revolutioniert die Sicherheitstests für neue Medikamente
Catrin Kabus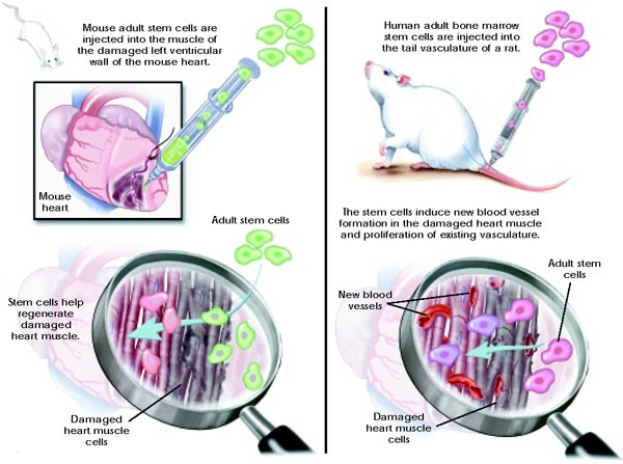
Mini-Herz aus dem Labor revolutioniert die Sicherheitstests für neue Medikamente
Wissenschaftler haben ein winziges, im Labor gezüchtetes Herzmodell entwickelt, das die Art und Weise verändern könnte, wie neue Medikamente getestet werden. Forscher des Fraunhofer-Instituts für Toxikologie und Experimentelle Medizin (ITEM) und der Medizinischen Hochschule Hannover (MHH) haben das Mini-Herz-Organoid geschaffen, um schädliche Nebenwirkungen auf das Herz bereits in einer frühen Phase der Medikamentenentwicklung zu erkennen. Im Gegensatz zu einfachen Zellkulturen ahmt dieses fortschrittliche Modell menschliches Herzgewebe weitaus präziser nach und bietet so eine bessere Möglichkeit, Risiken abzuschätzen, bevor Arzneimittel an Patienten verabreicht werden.
Die Mini-Herz-Organoide bestehen aus verschiedenen Zelltypen, darunter Herzmuskelzellen, Herzfibroblasten, Endothelzellen und mesenchymale Stammzellen. Alle diese Komponenten stammen aus induzierten pluripotenten menschlichen Stammzellen (iPS-Zellen), wodurch die Organoide dem echten Herzgewebe sehr ähnlich sind. Ein entscheidender Durchbruch ist die Integration eines Immunsystems in das Organoid, das es noch stärker wie ein menschliches Herz reagieren lässt als frühere Modelle.
Die Organoide überleben im Labor mindestens dreißig Tage, was den Forschern genug Zeit gibt, Langzeiteffekte zu untersuchen. Diese verlängerte Lebensdauer ist besonders nützlich für die Erprobung neuer Wirkstoffklassen, wie etwa RNA-Therapien, deren Wirkung sich oft erst nach Wochen zeigt. Zudem können Wissenschaftler die Organoide durch elektrische Impulse – ähnlich wie ein Herzschrittmacher – zur Kontraktion anregen, um zu beobachten, wie sie unter verschiedenen Bedingungen reagieren.
Erste Tests haben bereits gezeigt, dass die Organoide auf Medikamente ähnlich reagieren wie menschliche Herzen. So veränderte sich etwa die Kontraktionsfähigkeit der Organoide bei der Gabe bestimmter Arzneimittel, insbesondere bei solchen, die aus Zellen von Patienten mit hypertropher Kardiomyopathie erzeugt wurden. Die Forscher analysieren diese Reaktionen mithilfe von hochauflösender Schlagfrequenzmessung, Gewebeuntersuchungen und Einzelzell-Genexpressionsanalysen.
Kardiotoxizität ist eine der Hauptursachen für das Scheitern von Medikamenten und zwingt Unternehmen häufig dazu, vielversprechende Therapien in späten Entwicklungsphasen aufzugeben. Dieses neue Modell könnte helfen, Risiken früher zu erkennen, Kosten zu senken und die Sicherheit zu erhöhen. Zwei Fraunhofer-Institute waren an dem Projekt beteiligt, was seine Bedeutung für die Früherkennung in der Medikamentenforschung unterstreicht.
Das Herz-Organoid-Modell bietet eine präzisere Methode, um Medikamente auf schädliche Auswirkungen auf das Herz zu testen, noch bevor klinische Studien am Menschen beginnen. Durch die frühere Erkennung von Problemen könnten sowohl Zeit als auch Ressourcen in der Arzneimittelentwicklung eingespart werden. Die Technologie steht nun für die Erprobung neuer Wirkstoffe zur Verfügung und stellt ein leistungsstarkes Werkzeug für die pharmazeutische Forschung dar.